Western blot(蛋白印迹)作为科研研究中最为平常的实验,却蕴含了很多知识,可谓是小实验里却有大文章。尽管绝大多数研究僧在接触该实验时都会被虐的体无完肤,却也在和WB斗志斗勇的过程中积累了不少经验。正所谓前人种树,后人乘凉,现在小鱼就把各位前辈做WB的各种经验总结起来,希望对大家能有所帮助。
WB的基本原理
在电场的作用下将电泳分离的多肽从聚丙烯酰胺凝胶转移至一种固相支持体,然后用这种多肽的特异抗体来检测,经常用于目的蛋白的表达特性分析、组织定位、表达量分析及与其他蛋白的互作。依其原理,可分为两种方法:A、直接法和B、间接法。
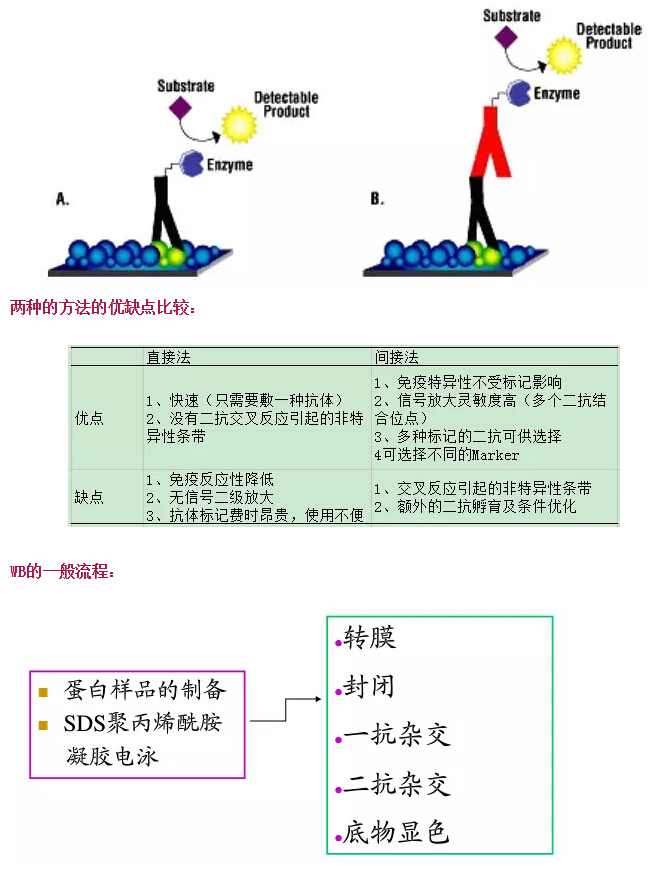
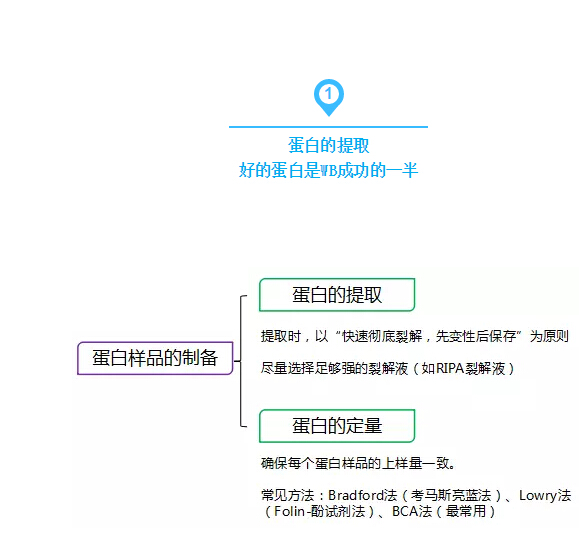
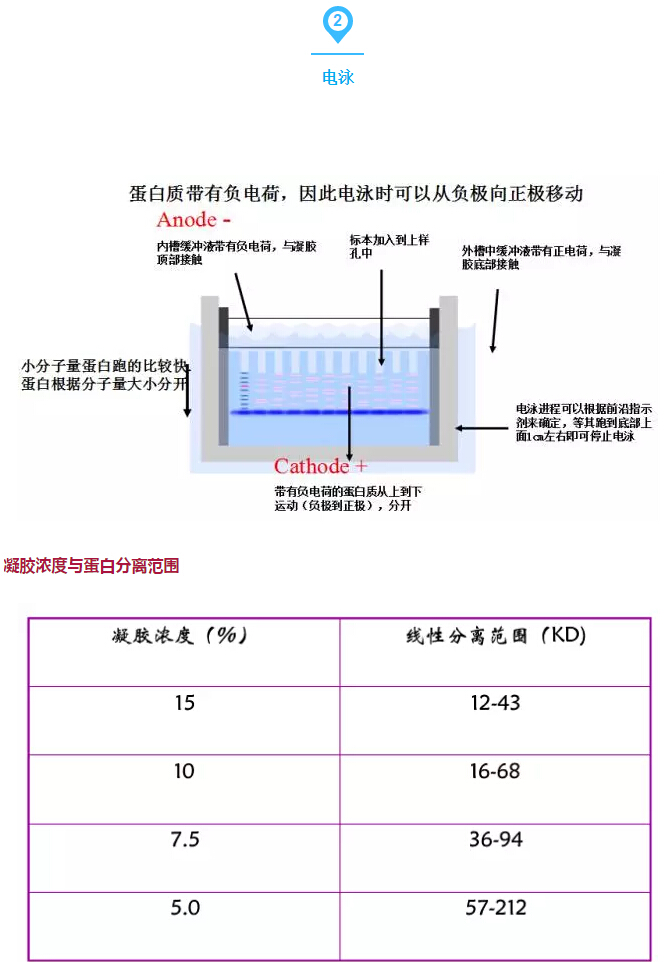
经验总结:
1:合适的盐浓度下,保持蛋白质的最大溶解性和可重复性。
2:尽量除去核酸,多糖,脂类等干扰分子
3:提取蛋白质过程中,应在低温环境下进行,以抑制蛋白酶的水解作用(可加入适合的蛋白酶抑制剂)。
4:蛋白样品建议分装后冷冻干燥或直接以液体态置-80℃中保存,不要反复冻融。
5:蛋白浓度低时,可使用超滤膜浓缩或者用真空冻干机将蛋白冻干。
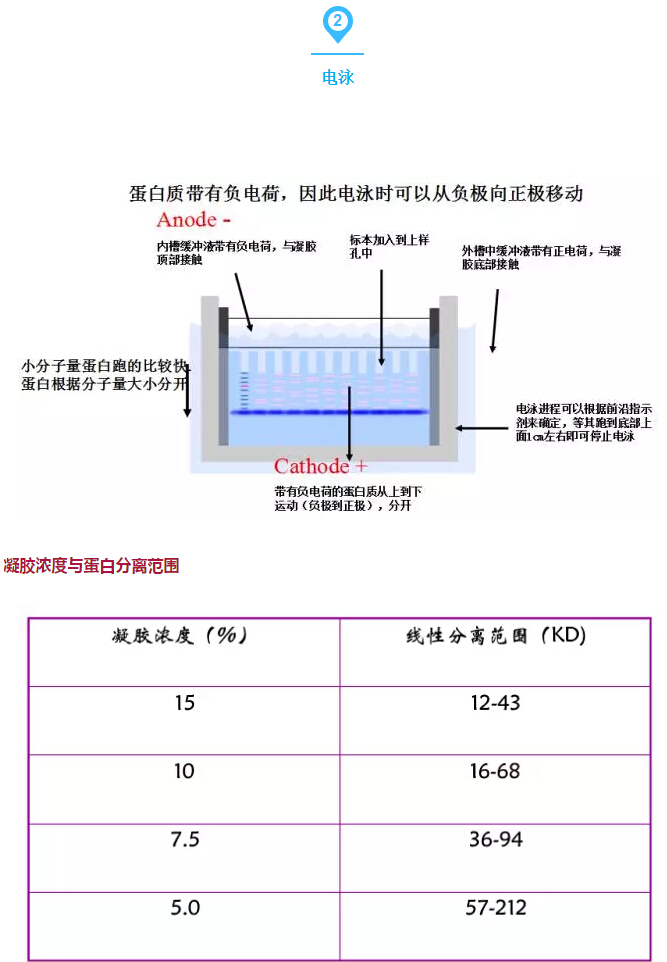
经验总结:
1:上样时:根据蛋白表达丰度调整蛋白上样量,尽量保证每孔上样量保持一致。
2:胶最好现配现用,如果需要保存,最好用湿润的保鲜膜包好并置于4℃冰箱中。
3:为了检测整个实验系统或校准实验结果,需要设置内参(一般指由管家基因编码表达的蛋白)。

4:为了确保western blot结果的准确性和特异性,设置合适正确的对照是必不可少,一般需要设置的对照如下——
阳性对照:明确表达检测蛋白的组织或细胞,用于检测抗体的工作效率;
阴性对照:明确不表达检测蛋白组织或细胞,用于检测抗体的特异性;
二抗对照:不加一抗,用于检测二抗的特异性;
内参对照:检测标本的质量和二抗系统
空白对照:不加一抗和二抗;用于检测膜的性质和封闭的效果。

用于western blot的杂交膜主要有两种:NC膜和PVDF膜,可依据目的蛋白与膜的结合能力及膜的孔径来挑选不同的转移膜。
两个膜之间的比较:
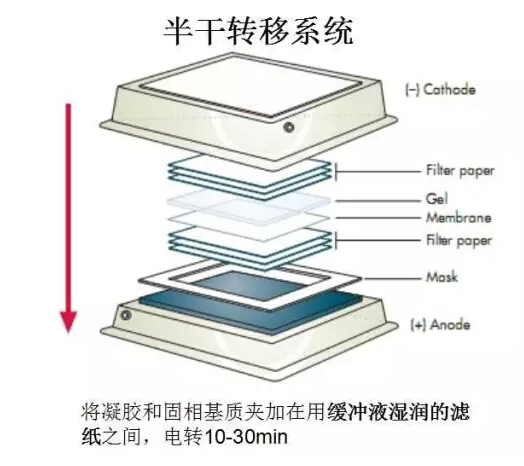
转膜方法:分为两种湿转法和半干法
经验总结:
1:胶在负极,膜靠近正极;滤纸不要大过膜,防止短路;
2:夹好膜和凝胶后,确定在凝胶、膜和滤纸之间没有气泡存在,否则会导致转膜不完全。
3:注意一定要戴手套或塑料镊子接触膜,避免手上的蛋白和油脂降低转膜效率。
4:转膜过程中,尤其是高电流快速转膜时,通常 会有非常严重的发热现象,最好把转膜槽放置在冰浴中进行转膜。
5:对于湿转法:一般转膜的电流在200mA-400mA之间,转膜时间为30-60分钟。也可以在15-20mA转膜过夜。大片段的>50KD的可以选用350mA,小片段的可以用250mA。具体的转膜时间要根据目的蛋白的大小而定,目的蛋白的分子量越大,需要的转膜时间越长,目的蛋白的分子量越小,需要的转膜时间越短。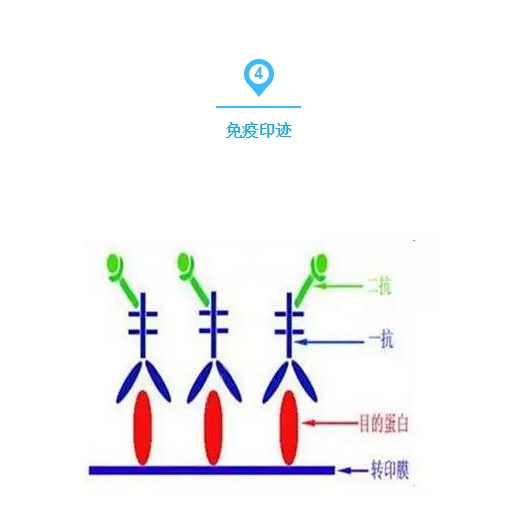
经验总结:
1:常见的封闭液有5%脱脂奶粉、BSA和Western Blot膜封闭液(生物试剂公司提供)。但是封闭液的选取具体得看抗体说明书,有的抗体是明确要求只能用BSA,而封闭液浓度的选择也是具体得看抗体的要求,但是一般情况5%BSA会比5%牛奶的效果好。
2:选择抗体时,一方面需要考虑所选抗体是否能识别凝胶电泳后转印至膜上的变性蛋白,另一方面需要考虑所选抗体是否会引起交叉反应条带。

WB做完后,有时需要对结果进行定量。然而最备受推崇的定量分析软件Quantiy One软件因其高昂的售价令很多人望而却步,但除了该软件外还有一个比较简单的图像处理软件ImageJ可以很方便的进行灰度和密度分析。
ImageJ的软件界面
1.ImageJ对WB条带进行灰度分析
1)File|Open打开WB结果图片
2)图片类型设置:Image|Type|8bit
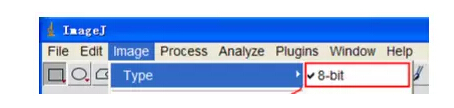
3)去除图片背景:Process|Subtract Background
在Subtract Background窗口按照以下条件进行设置:
4)设置定量参数:Analyze |SetMeasurements,点击Area,Mean Gray Value及Integrated Density
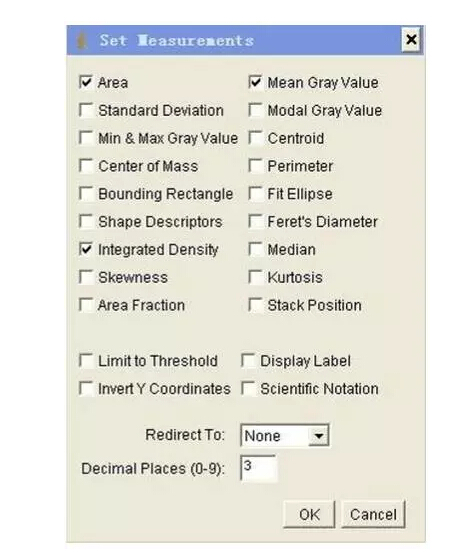
5)设置单位: Analyze|SetScale,在“unit of length”的方框里输入“pixels”
6)将图片转换成亮带,Edit|Invert

7)选择Freehand Selection,尽量把条带圈起来,点击键盘m,出来IntDen灰度值
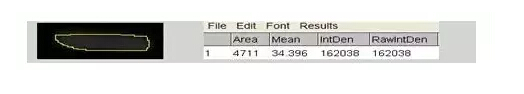
8)复制数据IntDen进行分析
2. Image J 对WB条带进行密度分析
1)步骤同前,File|Open打开WB结果图片
2)如果条带不正,需修正

Image transform rotate调节angle值,直到条带水平为止
3)选中矩形选项,圈中第一个条带,AnalyzeGels Select Firstlane(快捷键Ctrl +1),然后移动第一个条带上的矩形到第二个条带上,Analyze Gels Select Second Lane(快捷键Ctrl+2),最后Analyze GelPlotlanes

选中直线工具,将开口的波峰关闭

选中魔棒工具,点击波峰可以显示波峰下面积,即条带的密度值

以第一个数值为基数,其他数值与第一个数值的比值即为相对密度。

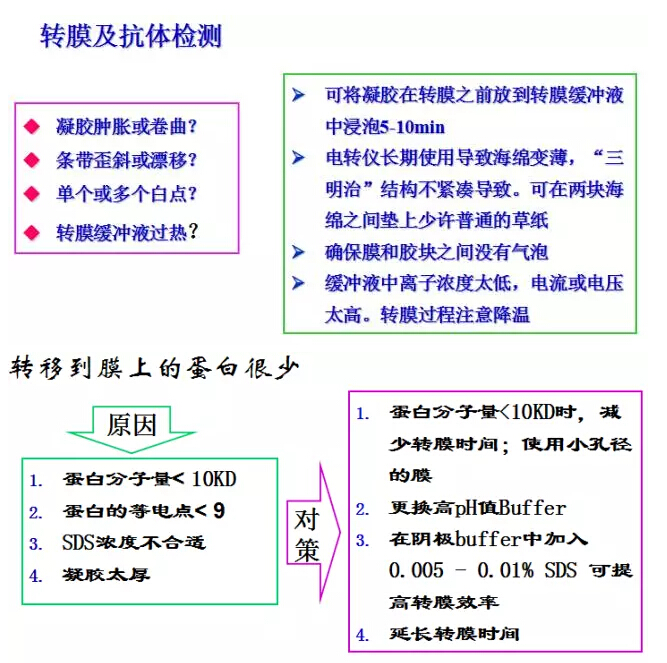
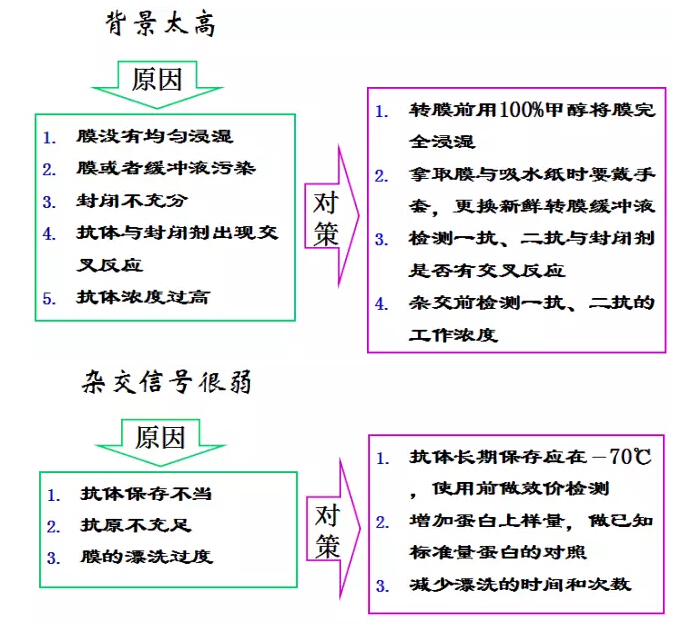
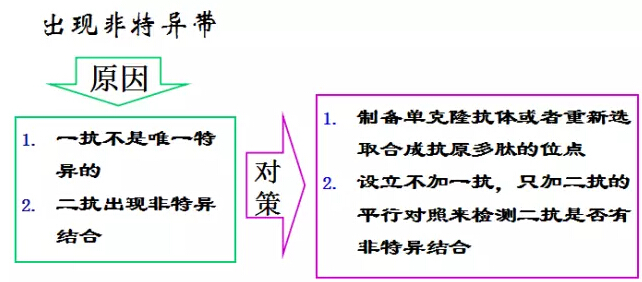
另附前辈们11条“济世”经验

1、抽提出某个蛋白第一次检测,因为不知道表达量咋样,可以减少裂解液(这样蛋白浓度高一些),上样量加大,抗体浓度大一点,增加出结果的几率,否则出不来结果不知道是因为蛋白量太小还是抗体等其他条件影响,有结果后再根据条带的亮度调整各种试剂的用量。
2、同时检测两种蛋白或两个样本的同种蛋白时,蛋白抽提出来后测浓度,调整每个孔的蛋白上样量一致,通常做法时,做标准曲线,再计算待测蛋白的浓度,下面是偷懒的办法:直接用酶标仪测这两个样品的吸光度,根据吸光度值将两个样品的蛋白浓度调整成一致后上样。吸光度跟蛋白浓度成正比,没必要一定要测量出具体浓度,而且只要使我研究的一对蛋白浓度调整一样(对照组,处理组),没必要将不同样本的各组均调节成一个浓度。(懒人有懒人的活法,但是我懒得有原则)
3、科研小白注意黑胶白膜,黑胶白膜,黑胶白膜,重要的事情说三遍。转膜是最好是将膜放在下面,胶放上面,否则会有镜像效果,等转完膜后拿出膜时,把膜反过来时,上样顺序会左右颠倒,因为胶无正反,膜有正反。
4、marker尽量不要放在中间,放在两边作为顺序的标记,或者,在胶剥离出来后和PVDF膜的一角剪掉一小块作为标记。(翻过来翻过去,咦,记不得哪边是哪边了)
5、封闭的时间可以延长问题不大,但是跑胶电泳时不能将胶长时间放在仪器里面,而应该放在转膜液里固定(里面有甲醛,可固定蛋白),如果在没有电流下蛋白一直在胶内 ,蛋白未被固定,会扩散,转完膜后条带难看。(甲醛是什么呀,就是大家经常报道的新装修的房子甲醛超标,所以实验狗不容易呀,每天跟这些有毒的东西打交道。)
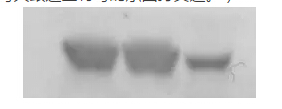
6、封闭不一定要使用脱脂牛奶,3%BSA也可以,做磷酸化蛋白是尽量使用BSA可以降低背景。一般的实验还是用便宜的脱脂牛奶。
7、如果一次性需要检测多个蛋白,电泳后可根据marker(即分子量)将膜剪开,分别不同的抗体孵育,可一次检测多个蛋白;当两个蛋白分子量很相近PVDF膜无法剪开时,可先曝表达弱的蛋白,再用抗体洗脱液将已结合的一抗、二抗洗去,这样一张印迹膜可以多次使用,再曝表达强的蛋白,但注意的是此种方法可由于剧烈处理丢失某些表位。
8、买一个抗体孵育槽可以节省抗体的使用量,每个小槽可以孵一张膜。(土豪请忽略这一条,哪里买,问淘宝)

9、内参因为使用量大,市面上有带HRP的内参出售(言外之意就是一抗上面就带HRP,就不用孵二抗了),前几次摸条件时,用带HRP的内参,可以直接一抗后先曝下内参,如果内参不齐,目的基因暂时就不用孵育了,等调节蛋白上样量一致后再去检测目的基因。
10、抽提蛋白时全程都要在冰上, 因为加了细胞裂解液后细胞被破坏,细胞内的各种酶被释放,如果不在冰上操作,蛋白容易降解,如果开始抽提蛋白,建议一次性操作到加上loading buffer煮蛋白变性的步骤,煮蛋白的将蛋白变性,后不易降解,如果要长期保存,放到-20度。
11、频繁做WB时,可以一次可以多配几块电泳胶,running buffer 4度保存,省的每次配胶。
